यूनिट 13 ऐमीन (क्रमशः प्रश्न)
प्रश्न
13.1 निम्नलिखित यौगिकों के IUPAC नाम लिखिए तथा उन्हें प्राथमिक, द्वितीयक एवं तृतीयक ऐमीन में वर्गीकृत कीजिए।
(i) $\left({CH_3}\right)_{2} {CHNH_2}$
(ii) ${CH_3}\left({CH_2}\right)_{2} {NH_2}$
(iii) ${CH_3} {NHCH}\left({CH_3}\right)_{2}$
(iv) $\left({CH_3}\right)_{3} {CNH_2}$
(v) ${C_6} {H_5} {NHCH_3}$
(vi) $\left({CH_3} {CH_2}\right)_{2} {NCH_3}$
(vii) $m-{BrC_6} {H_4} {NH_2}$
उत्तर दिखाएँ
उत्तर
(i) 1-मेथिल ऐथेनामीन ( $1^{\circ}$ ऐमीन)
(ii) प्रोपेन-1-ऐमीन ( $1^{\circ}$ ऐमीन)
(iii) N-मेथिल-2-मेथिल ऐथेनामीन ( $2^{\circ}$ ऐमीन)
(iv) 2-मेथिल प्रोपेन-2-ऐमीन ( $1^{\circ}$ ऐमीन)
(v) N-मेथिल बेंज़ोइन ऐमीन या ${N}$-मेथिल ऐनिलीन ($2^{\circ}$ ऐमीन)
(vi) ${N}$-एथिल- ${N}$-मेथिल ऐथेनामीन ( $3^{\circ}$ ऐमीन)
(vii) 3-ब्रोमो बेंज़ेनामीन या 3-ब्रोमो ऐनिलीन ( $1^{\circ}$ ऐमीन)
13.2 निम्नलिखित यौगिकों के युग्म के बीच अंतर के लिए एक रासायनिक परीक्षण दीजिए।
(i) मेथिल ऐमीन एवं डाइमेथिल ऐमीन
(ii) द्वितीयक एवं तृतीयक ऐमीन
(iii) एथिल ऐमीन एवं ऐनिलीन
(iv) ऐनिलीन एवं बेंजिल ऐमीन
(v) ऐनिलीन एवं ${N}$-मेथिल ऐनिलीन।
उत्तर दिखाएँ
उत्तर
(i) मेथिल ऐमीन एवं डाइमेथिल ऐमीन के बीच अंतर के लिए कार्बिलऐमीन परीक्षण का उपयोग किया जा सकता है।
एलिफैटिक एवं ऐरोमैटिक प्राथमिक ऐमीन एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ गर्म करने पर खासी गंध वाले आइसोसाइनाइड या कार्बिलऐमीन बनाते हैं। मेथिल ऐमीन (एलिफैटिक प्राथमिक ऐमीन होने के कारण) कार्बिलऐमीन परीक्षण में धनात्मक परिणाम देता है, लेकिन डाइमेथिल ऐमीन नहीं।
(ii) द्वितीयक एवं तृतीयक ऐमीन के बीच अंतर के लिए उन्हें हिंसबर्ग के अभिकर्मक (बेंज़ीन सल्फोनिल क्लोराइड, ${C_6} {H_5} {SO_2} {Cl}$) के साथ अभिक्रिया कराई जा सकती है।
द्वितीयक ऐमीन हिंसबर्ग के अभिकर्मक के साथ अभिक्रिया करके एक उत्पाद बनाती है जो किसी क्षारक में अघुलनशील होता है। उदाहरण के लिए, N, N - डाइएथिल ऐमीन हिंसबर्ग के अभिकर्मक के साथ अभिक्रिया करके N, N डाइएथिल बेंज़ोइन सल्फोनामाइड बनाती है, जो किसी क्षारक में अघुलनशील होता है। तृतीयक ऐमीन के लिए इस अभिकर्मक के साथ कोई अभिक्रिया नहीं होती।
(iii) एथिलामीन और एनिलीन को एजो-डाइ के परीक्षण के माध्यम से अलग किया जा सकता है।
जब औषधीय एमीन एनिलीन के साथ ${HNO_2}\left({NaNO_2}+\right.$ तनु $\left.{HCl}\right)$ के साथ $0-5^{\circ} {C}$ पर अभिक्रिया करते हैं, तो एक डाइ क प्राप्त होता है, जिसके बाद इसे 2-नैफ्थॉल के क्षारीय विलयन के साथ अभिक्रिया कराई जाती है। डाइ क आमतौर पर पीला, लाल या अंगूर के रंग का होता है। एलिफैटिक एमीन इसी परिस्थितियों में ${N_2}$ गैस के उत्सर्जन के कारण तेज उत्सर्जन देते हैं।
(iv) एनिलीन और बेंजिल एमीन को नाइट्रस अम्ल के माध्यम से अपने प्रतिक्रियाओं की सहायता से अलग किया जा सकता है, जो एक खनिज अम्ल और सोडियम नाइट्राइट से स्थानीय रूप से बनाया जाता है। बेंजिल एमीन नाइट्रस अम्ल के साथ अभिक्रिया करके अस्थायी डाइजोनियम लवण बनाता है, जो फिर नाइट्रोजन गैस के उत्सर्जन के साथ एल्कोहल देता है।
दूसरी ओर, एनिलीन के ${HNO_2}$ के साथ निम्न तापमान पर अभिक्रिया करके स्थायी डाइजोनियम लवण बनाता है। इसलिए नाइट्रोजन गैस के उत्सर्जन के लिए नहीं होता।
(v) एनिलीन और N-मेथिल एनिलीन को कार्बिलैमीन परीक्षण के माध्यम से अलग किया जा सकता है।
प्राथमिक एमीन चलोरोफॉर्म और एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ गरम करने पर गंध वाले आइसोसाइनाइड या कार्बिलैमीन बनाते हैं। एनिलीन, जो एक औषधीय प्राथमिक एमीन है, कार्बिलैमीन परीक्षण में धनात्मक परिणाम देता है। हालांकि, N-मेथिल एनिलीन, जो एक द्वितीयक एमीन है, इस परीक्षण में धनात्मक परिणाम नहीं देता।
13.3 निम्नलिखित के बारे में बताइए:
(i) एनिलीन के ${pK_b}$ मेथिल एमीन के ${pK_b}$ से अधिक होता है।
(ii) एथिलामीन पानी में घुलनशील होता है जबकि एनिलीन नहीं।
(iii) मेथिल एमीन पानी में फेरिक क्लोराइड के साथ अभिक्रिया करके जलयुक्त फेरिक ऑक्साइड के अवक्षेप के रूप में अभिक्रिया करता है।
(iv) एमीन ग्रुप औषधीय विस्थापन अभिक्रियाओं में $O-$ और $p$ - दिशा देता है, लेकिन एनिलीन के नाइट्रेशन के दौरान m-नाइट्रोएनिलीन के एक बड़ी मात्रा में उत्पादन होता है।
(v) एनिलीन फ्रेडेल-क्राफ्ट्स अभिक्रिया में भाग नहीं लेता।
(vi) औषधीय एमीन के डाइजोनियम लवण एलिफैटिक एमीन के डाइजोनियम लवण से अधिक स्थायी होते हैं।
(vii) गैब्रियल फ्थैलिमाइड संश्लेषण प्राथमिक एमीन के संश्लेषण के लिए अधिक पसंद किया जाता है।
उत्तर दिखाएं
Answer
(i) एनिलीन के ${p} K_{b}$ मेथिल एमीन के ${p} K_{b}$ से अधिक होता है :

एनिलीन रेजोनेंस के कारण अनुभव करता है और इसके कारण, ${N}$-परमाणु पर इलेक्ट्रॉन बेंजीन वलय पर वितरित हो जाते हैं। इसलिए, ${N}$-परमाणु पर इलेक्ट्रॉन ज्यादा दान करने के लिए उपलब्ध नहीं होते।

दूसरी ओर, मेथिलएमीन के मामले में (मेथिल समूह के $+{I}$ प्रभाव के कारण), ${N}$-परमाणु पर इलेक्ट्रॉन घनत्व बढ़ जाता है। इस कारण, एनिलीन मेथिलएमीन की तुलना में कम क्षारकीय होता है। इसलिए, एनिलीन का $p K_{b}$ मेथिलएमीन के $p K_{b}$ से अधिक होता है।
(ii) एथिलएमीन पानी में घुलनशील होता है जबकि एनिलीन नहीं :
एथिलएमीन पानी में मिलाए जाने पर जल के साथ अंतरमoleculer ${H}$ - बंधन बनाता है। इसलिए, यह पानी में घुलनशील होता है।

लेकिन एनिलीन के कारण बड़े जल-अप्रतिरोधी - ${C_6} {H_5}$ समूह के उपस्थिति के कारण, एनिलीन पानी के साथ ${H}$ - बंधन के लिए बहुत कम अनुभव करता है। इसलिए, एनिलीन पानी में घुलनशील नहीं होता है।
(iii) मेथिलएमीन पानी में फेरिक क्लोराइड के साथ अभिक्रिया करके जलयुक्त फेरिक ऑक्साइड के अवक्षेप का निर्माण करता है :
मेथिल समूह के $+{I}$ प्रभाव के कारण, मेथिलएमीन पानी की तुलना में अधिक क्षारकीय होता है। इसलिए, पानी में मेथिलएमीन, पानी से ${H}^{+}$ आयन लेकर ${OH^-}$ आयन उत्पन्न करता है।
$ {CH_3}-{NH_2}+{H}-{OH} \longrightarrow {CH_3}-\stackrel{+}{{N}} {H_3}+{OH}^{-} $
फेरिक क्लोराइड $\left({FeCl_3}\right)$ पानी में विघटित होकर ${Fe}^{3+}$ और ${Cl^-}$ आयन बनाता है।
$ {FeCl_3} \longrightarrow {Fe}^{3+}+3 {Cl}^{-} $
फिर, ${OH^-}$ आयन ${Fe}^{3+}$ आयन के साथ अभिक्रिया करता है और जलयुक्त लोहा ऑक्साइड के अवक्षेप का निर्माण करता है।
$ 2 {Fe}^{3+}+6 {OH}^{-} \longrightarrow \underset{{\substack{\text{Hydrated}\\ \text{ferric oxide}}}}{{Fe_2} {O_3} \cdot 3 {H_2} {O}} $
(iv) हालांकि, ऐमीनो समूह औषधीय विस्थापन अभिक्रियाओं में $o-, p$ - दिशात्मक होता है, लेकिन एनिलीन के नाइट्रेशन से $m$-नाइट्रोएनिलीन के एक बड़े मात्रा में निर्माण होता है:
नाइट्रेशन अम्लीय माध्यम में किया जाता है। अम्लीय माध्यम में, एनिलीन के प्रोटॉनिकरण से एनिलिनियम आयन (जो मेटा-दिशात्मक होता है) बनता है।

इस कारण से, एनिलीन के नाइट्रेशन से $m$-नाइट्रोएनिलीन के एक बड़े मात्रा में निर्माण होता है।
(v) एनिलीन फ्रीडल-क्राफ्ट्स अभिक्रिया में भाग नहीं लेता है:
फ्रीडल-क्राफ्ट्स अभिक्रिया ${AlCl_3}$ की उपस्थिति में किया जाता है। लेकिन ${AlCl_3}$ प्रकृति में अम्लीय होता है, जबकि एनिलीन एक मजबूत क्षार होता है। इसलिए, एनिलीन ${AlCl_3}$ के साथ अभिक्रिया करके एक लवण बनाता है (जैसा कि नीचे दिए गए समीकरण में दिखाया गया है)।

$N$-परमाणु पर धनावेश के कारण, बेंजीन वलय में विस्थापन अभिक्रिया अक्रिय हो जाती है। इसलिए, एनिलीन फ्रीडल-क्राफ्ट्स अभिक्रिया में भाग नहीं लेता है।
(vi) औषधीय ऐमीन के डाइऐजोनियम लवण अलिफैटिक ऐमीन के डाइऐजोनियम लवण से अधिक स्थायी होते हैं:
डाइऐजोनियम आयन नीचे दिखाए गए तरीके से रेजोनेंस करता है:

इस रेजोनेंस के कारण डाइऐजोनियम आयन की स्थायिता होती है। इसलिए, औषधीय ऐमीन के डाइऐजोनियम लवण अलिफैटिक ऐमीन के डाइऐजोनियम लवण से अधिक स्थायी होते हैं।
(vii) गैब्रियल फ्थैलिमाइड संश्लेषण प्राथमिक ऐमीन के संश्लेषण के लिए पसंद किया जाता है :
गैब्रियल संश्लेषण प्राथमिक ऐमीन के निर्माण के लिए प्रयोग किया जाता है। फ्थैलिमाइड एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ उपचार प्राप्त करता है जो फ्थैलिमाइड के पोटैशियम लवण का निर्माण करता है जो अल्किल हैलाइड के साथ गर्म करने के बाद क्षारीय हाइड्रोलिज़िस के परिणामस्वरूप संगत प्राथमिक ऐमीन उत्पन्न करता है। ऐरोमैटिक प्राथमिक ऐमीन इस विधि द्वारा नहीं बनाए जा सकते क्योंकि ऐरिल हैलाइड फ्थैलिमाइड द्वारा बनाए गए एनियन के साथ न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया नहीं करते हैं।

13.4 निम्नलिखित को व्यवस्थित करें:
(i) ${p} K_{b}$ मान के घटते क्रम में:
${C_2} {H_5} {NH_2}, {C_6} {H_5} {NHCH_3},\left({C_2} {H_5}\right)_{2} {NH}$ और ${C_6} {H_5} {NH_2}$
(ii) क्षारकता के बढ़ते क्रम में:
${C_6} {H_5} {NH_2}, {C_6} {H_5} {~N}\left({CH_3}\right)_{2},\left({C_2} {H_5}\right)_2 {NH}$ और ${CH_3} {NH_2}$
(iii) क्षारकता के बढ़ते क्रम में:
(a) एनिलीन, $p$-नाइट्रोएनिलीन और $p$-टॉल्यूडीन
(b) ${C_6} {H_5} {NH_2}, {C_6} {H_5} {NHCH_3}, {C_6} {H_5} {CH_2} {NH_2}$.
(iv) गैस अवस्था में क्षारकता के घटते क्रम में:
${C_2} {H_5} {NH_2},\left({C_2} {H_5}\right)_2 {NH},\left({C_2} {H_5}\right)_3 {~N}$ और ${NH_3}$
(v) क्वथनांक के बढ़ते क्रम में:
${C_2} {H_5} {OH},\left({CH_3}\right)_{2} {NH}, {C_2} {H_5} {NH_2}$
(vi) पानी में विलेयता के बढ़ते क्रम में:
${C_6} {H_5} {NH_2},\left({C_2} {H_5}\right)_{2} {NH}, {C_2} {H_5} {NH_2}$.
उत्तर दिखाएं
Answer
(i) ${C _2} {H _5} {NH _2}$ में केवल एक $-{C _2} {H _5}$ समूह होता है जबकि $\left({C _2} {H _5}\right) _{2} {NH}$ में दो $-{C _2} {H _5}$ समूह होते हैं। इसलिए, $\left({C _2} {H _5}\right) _{2} {NH}$ में $+{I}$ प्रभाव $\left({C _2} {H _5}\right) _{2} {NH}$ में ${C _2} {H _5} {NH _2}$ की तुलना में अधिक होता है। इसलिए, ${N}$-परमाणु पर इलेक्ट्रॉन घनत्व $\left({C _2} {H _5}\right) _{2} {NH}$ में ${C _2} {H _5} {NH _2}$ की तुलना में अधिक होता है। अतः $\left({C _2} {H _5}\right) _{2} {NH}$ ${C _2} {H_5} {NH_2}$ की तुलना में अधिक क्षारक होता है।
भी, ${C_6} {H_5} {NHCH_3}$ और ${C_6} {H_5} {NH_2}$ दोनों कम मूलक हैं जैसे कि $\left({C_2} {H_5}\right)_{2} {NH}$ और ${C_2} {H_5} {NH_2}$ के मुकाबले क्योंकि पहले दो में अकेले युग्म इलेक्ट्रॉन के वितरण के कारण है। इसके अलावा, ${C_6} {H_5} {NHCH_3}$ और ${C_6} {H_5} {NH_2}$ में से पहले वाला $-{CH_3}$ समूह के $+{I}$ प्रभाव के कारण अधिक मूलक होगा। इसलिए, दिए गए यौगिकों के मूलकता के बढ़ते क्रम निम्नलिखित हैं:
${C_6} {H_5} {NH_2}<{C_6} {H_5} {NHCH_3}<{C_2} {H_5} {NH_2}<\left({C_2} {H_5}\right)_{2} {NH}$
हम जानते हैं कि मूलकता के बढ़ते होने पर ${p} K_{b}$ मान कम होते हैं।
${C_6} {H_5} {NH_2}>{C_6} {H_5} {NHCH_3}>{C_2} {H_5} {NH_2}>\left({C_2} {H_5}\right)_{2} {NH}$
(ii) ${C _6} {H _5} {~N}\left({CH _3}\right) _{2}$, ${C _6} {H _5} {NH _2}$ की तुलना में अधिक मूलक है क्योंकि ${C _6} {H _5} {~N}\left({CH _3}\right) _{2}$ में दो ${CH _3}$ समूहों के $+{I}$ प्रभाव के कारण है। इसके अलावा, ${CH _3} {NH _2}$ में एक $-{CH _3}$ समूह होता है जबकि $\left({C _2} {H _5}\right) _{2} {NH}$ में दो $-{C _2} {H _5}$ समूह होते हैं। इसलिए, $\left({C _2} {H _5}\right) _{2} {NH}$, ${C _2} {H _5} {NH _2}$ की तुलना में अधिक मूलक है।
अब, ${C_6} {H_5} {~N}\left({CH_3}\right)_{2}$, ${CH_3} {NH_2}$ की तुलना में कम मूलक है क्योंकि $-{C_6} {H_5}$ समूह के -R प्रभाव के कारण है।
इसलिए, दिए गए यौगिकों के मूलकता के बढ़ते क्रम निम्नलिखित हैं:
${C _6} {H _5} {NH _2}<{C _6} {H _5} {~N}\left({CH _3}\right) _{2}<{CH _3} { NH _2}<\left({C _2} { H _5}\right) _{2} {NH}$
(iii)
(a)

$ p $-टॉल्यूडीन में, इलेक्ट्रॉन-दाता $-{CH_3}$ समूह की उपस्थिति नाइट्रोजन परमाणु पर इलेक्ट्रॉन घनत्व को बढ़ाती है। इसलिए, $ p $-टॉल्यूडीन, एनिलीन की तुलना में अधिक मूलक है।
दूसरी ओर, $ p $-नाइट्रोएनिलीन में इलेक्ट्रॉन-घीरा $-{NO_2}$ समूह की उपस्थिति नाइट्रोजन परमाणु पर इलेक्ट्रॉन घनत्व को कम करती है। इसलिए, $ p $-नाइट्रोएनिलीन, एनिलीन की तुलना में कम मूलक है।
अतः, दिए गए यौगिकों के बेसिक शक्ति के बढ़ते क्रम निम्नलिखित है:
$ p $-नाइट्रोएनिलीन $ < $ एनिलीन $ < p $-टॉल्यूडीन
(b) ${C_6} {H_5} {NHCH_3}$, ${C_6} {H_5} {NH_2}$ की तुलना में अधिक बेसिक है क्योंकि ${C_6} {H_5} {NHCH_3}$ में इलेक्ट्रॉन-दाता -${CH_3}$ समूह उपस्थित है।
फिर, ${C_6} {H_5} {NHCH_3}$ में -${C_6} {H_5}$ समूह ${N}$-परमाणु के सीधे जुड़ा हुआ है। हालांकि, ${C_6} {H_5} {CH_2} {NH_2}$ में ऐसा नहीं है। अतः, ${C_6} {H_5} {NHCH_3}$ में -${R}$ प्रभाव के कारण ${C_6} {H_5}$ समूह के कारण ${N}$-परमाणु पर इलेक्ट्रॉन घनत्व कम हो जाता है। अतः, ${C_6} {H_5} {CH_2} {NH_2}$, ${C_6} {H_5} {NHCH_3}$ की तुलना में अधिक बेसिक है।
अतः, दिए गए यौगिकों के बेसिक शक्ति के बढ़ते क्रम निम्नलिखित है:
${C_6} {H_5} {NH_2} < {C_6} {H_5} {NHCH_3} < {C_6} {H_5} {CH_2} {NH_2}$.
(iv) गैस अवस्था में, सॉल्वेशन प्रभाव नहीं होता। अतः, बेसिक शक्ति मुख्य रूप से $+{I}$ प्रभाव पर निर्भर करती है। $+{I}$ प्रभाव जितना अधिक होता है, बेसिक शक्ति उतनी ही अधिक होती है। इसके अतिरिक्त, अल्किल समूहों की संख्या जितनी अधिक होती है, $+{I}$ प्रभाव उतना ही अधिक होता है। अतः, गैस अवस्था में दिए गए यौगिकों के बेसिक शक्ति के घटते क्रम निम्नलिखित है:
$\left({C _2} {H _5}\right) _{3} {~N}>\left({C _2} {H _5}\right) _{2} {NH}>{C _2} {H _5} {NH _2}>{NH _3}$
(v) यौगिकों के क्वथनांक उस यौगिक में उपस्थित ${H}$-बंध के विस्तार पर निर्भर करते हैं। यौगिक में ${H}$-बंध के अधिक विस्तार होने पर क्वथनांक अधिक होता है। $\left({CH _3}\right) _{2} {NH}$ में केवल एक ${H}$-परमाणु होता है जबकि ${C _2} {H _5} {NH _2}$ में दो ${H}$-परमाणु होते हैं। अतः, ${C _2} {H _5} {NH _2}$, $\left({CH _3}\right) _{2} {NH}$ की तुलना में अधिक विस्तारपूर्वक ${H}$-बंध करता है। अतः, ${C _2} {H _5} {NH _2}$ का क्वथनांक $\left({CH _3}\right) _{2} {NH}$ के क्वथनांक से अधिक होता है।
इसके अतिरिक्त, ${O}$, ${N}$ की तुलना में अधिक विद्युत ऋणात्मक होता है। अतः, ${C_2} {H_5} {OH}$, ${C_2} {H_5} {NH_2}$ की तुलना में अधिक मजबूत ${H}$-बंध बनाता है। अतः, ${C_2} {H_5} {OH}$ का क्वथनांक ${C_2} {H_5} {NH_2}$ और $\left({CH_3}\right)_{2} {NH}$ के क्वथनांक से अधिक होता है।
अब, दिए गए यौगिकों को उनके क्वथनांक के बढ़ते क्रम में निम्नलिखित तरीके से व्यवस्थित किया जा सकता है:
$\left({CH_3}\right)_{2} {NH}<{C_2} {H_5} {NH_2}<{C_2} {H_5} {OH}$
(vi) जितना अधिक H-बंधन होता है, उतनी अधिक विलेयता होती है। ${C _2} {H _5} {NH _2}$ में दो ${H}$ परमाणु होते हैं जबकि $\left({C _2} {H _5}\right) _{2} {NH}$ में केवल एक ${H}$ परमाणु होता है। अतः, ${C _2} {H _5} {NH _2}$ के अपेक्षाकृत अधिक H-बंधन होता है। इसलिए, ${C _2} {H _5} {NH _2}$ की पानी में विलेयता $\left({C _2} {H _5}\right) _{2} {NH}$ की तुलना में अधिक होती है।
इसके अतिरिक्त, ऐमीनों की विलेयता अणुभार के बढ़ते साथ कम हो जाती है। इसका कारण यह है कि ऐमीनों के अणुभार उनके हाइड्रोफोबिक भाग के आकार के बढ़ते साथ बढ़ता है। ${C_6} {H_5} {NH_2}$ का अणुभार ${C_2} {H_5} {NH_2}$ और $\left({C_2} {H_5}\right)_{2} {NH}$ के अणुभार से अधिक होता है।
अतः, उनकी पानी में विलेयता के बढ़ते क्रम निम्नलिखित है:
${C_6} {H_5} {NH_2}<\left({C_2} {H_5}\right)_{2} {NH}<{C_2} {H_5} {NH_2}$
13.5 आप कैसे बदलेंगे:
(i) एथेनोइक अम्ल को मेथेनामीन में
(ii) हेक्जेनिट्राइल को 1-एमिनोपेंटेन में
(iii) मेथनॉल को एथेनोइक अम्ल में
(iv) एथेनामीन को मेथेनामीन में
(v) एथेनोइक अम्ल को प्रोपेनोइक अम्ल में
(vi) मेथेनामीन को एथेनामीन में
(vii) नाइट्रोमेथेन को डाइमेथिलएमीन में
(viii) प्रोपेनोइक अम्ल को एथेनोइक अम्ल में?
उत्तर दिखाएं
Answer
(i)

(ii)

(iii)

(iv)

(v)

(vi)

(vii)

(viii)

13.6 प्राथमिक, द्वितीयक एवं तृतीयक ऐमीन की पहचान के लिए एक विधि का वर्णन करें। संलग्न रासायनिक अभिक्रियाओं के रासायनिक समीकरण भी लिखें।
उत्तर दिखाएं
उत्तर
बेंज़ीन सल्फोनिल क्लोराइड $\left({C}_6 {H}_5 {SO}_2 {Cl}\right)$, जिसे भी हिंसबर्ग अभिकर्मक के रूप में जाना जाता है, प्राथमिक एवं द्वितीयक ऐमीन के साथ अभिक्रिया करके सल्फोनामाइड बनाता है।
(a) बेंजीन सल्फोनिल क्लोराइड के प्राथमिक ऐमीन के साथ अभिक्रिया से एन-एथिल बेंजीन सल्फोनामाइड बनता है।

सल्फोनामाइड में नाइट्रोजन पर बंधे हुए हाइड्रोजन के कारण तीव्र विद्युत अपघटक सल्फोनिल समूह की उपस्थिति के कारण अत्यधिक अम्लीय होता है। इसलिए, इसका क्षारक में घुलनशीलता होती है।
(b) द्वितीयक ऐमीन के साथ अभिक्रिया में, एन, एन-डाइएथिलबेंज़ीन सल्फोनैमाइड बनता है।

क्योंकि एन, एन-डाइएथिलबेंज़ीन सल्फोनैमाइड में नाइट्रोजन परमाणु के संगत कोई भी हाइड्रोजन परमाणु नहीं होता है, इसलिए इसकी अम्लता नहीं होती है और इसलिए इसका क्षारक में विलेयता नहीं होती है।
(c) तृतीयक ऐमीन बेंज़ीन सल्फोनिल क्लोराइड के साथ अभिक्रिया नहीं करते हैं। ऐमीन के बेंज़ीन सल्फोनिल क्लोराइड के साथ अलग-अलग तरीके से अभिक्रिया करने की इस गुणता का उपयोग प्राथमिक, द्वितीयक और तृतीयक ऐमीन के अंतर के लिए और ऐमीन के मिश्रण के अलग करने के लिए किया जाता है। हालांकि, आजकल बेंज़ीन सल्फोनिल क्लोराइड के स्थान पर $p$-टॉल्यूईन सल्फोनिल क्लोराइड का उपयोग किया जाता है।
13.7 निम्नलिखित पर छोटे टिप्पणी लिखें:
(i) कार्बिलामीन अभिक्रिया
(ii) डाइजोटीकरण
(iii) होफमैन के ब्रोमामाइड अभिक्रिया
(iv) क्यूपिंग अभिक्रिया
(v) ऐमोनोलिसिस
(vi) ऐसीटिलेशन
(vii) गैब्रियल फ्थैलिमाइड संश्लेषण।
उत्तर दिखाएं
उत्तर
(i) कार्बिलामीन अभिक्रिया
एलिफैटिक और ऐरोमैटिक प्राथमिक ऐमीन चलोरोफॉर्म और एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ गरम करने पर आइसोसाइनाइड या कार्बिलामीन बनते हैं जो खासकर गंध वाले पदार्थ होते हैं। द्वितीयक और तृतीयक ऐमीन इस अभिक्रिया के लिए नहीं दिखाते हैं। यह अभिक्रिया कार्बिलामीन अभिक्रिया या आइसोसाइनाइड परीक्षण के रूप में जानी जाती है और यह प्राथमिक ऐमीन के परीक्षण के लिए उपयोग की जाती है।
$ \underset{\text{प्राथमिक ऐमीन}}{{R}-{NH_2}}+\underset{\text{क्लोरोफॉर्म}}{{CHCl_3}}+\underset{\substack{\text{पोटैशियम}\\ \text{हाइड्रॉक्साइड}}}{3 {KOH}(\text {एल्क. })} \xrightarrow{\Delta} \underset{\text{कार्बिलामीन}}{{R}-{NC}}+3 {KCl}+3 {H_2} {O} $
उदाहरण के लिए,
$ \underset{\text{मेथेनामीन}}{{CH_3}-{NH_2}}+{CHCl_3}+3 {KOH}(\text {एल्क.}) \xrightarrow{\Delta} \underset{\substack{\text{मेथिल कार्बिलामीन}\\ \text{या मेथिल आइसोसाइनाइड}}}{{CH_3}-{NC}}+3 {KCl}+3 {H_2} {O} $
(ii) डाइजोटीकरण
ऐरोमैटिक प्राथमिक ऐमीन नाइट्रस अम्ल (जो ${NaNO_2}$ और एक खनिज अम्ल जैसे ${HCl}$ से स्थानीय रूप से बनाया जाता है) के साथ निम्न तापमान (273-278 K) पर डाइजोनियम लवण बनाते हैं। ऐरोमैटिक प्राथमिक ऐमीन के डाइजोनियम लवण में बदले जाने की इस परिवर्तन को डाइजोटीकरण कहा जाता है।
उदाहरण के लिए, ${NaNO_2}$ और ${HCl}$ के साथ $273 - 278 {~K}$ पर उपचार के दौरान, एनिलीन बेंज़ीन डाइजियोनियम क्लोराइड उत्पन्न करती है, जिसके साथ ${NaCl}$ और ${H_2} {O}$ अपशिष्ट उत्पाद होते हैं।

(iii) हॉफमैन ब्रोमएमाइड अभिक्रिया
जब एमाइड को सोडियम हाइड्रॉक्साइड के जलीय या एथेनॉलिक घोल में ब्रोमीन के साथ उपचार किया जाता है, तो वास्तविक एमाइड की तुलना में एक कार्बन कम वाला प्राथमिक एमीन उत्पन्न होता है। इस अपघटन अभिक्रिया को हॉफमैन ब्रोमएमाइड अभिक्रिया के रूप में जाना जाता है। इस अभिक्रिया में एमाइड के कार्बोनिल कार्बन पर एक ऐल्किल या ऐरिल समूह नाइट्रोजन पर चला जाता है।

उदाहरण के लिए,

(iv) क्लॉपिंग अभिक्रिया
प्राप्त एजो उत्पादों में एक विस्तारित संयोजन प्रणाली होती है जिसमें दोनों ऐरोमैटिक वलय $-{N}={N}$ - बंध के माध्यम से जुड़े होते हैं। ये यौगिक अक्सर रंगीन होते हैं और डाइज़ बनाने के लिए उपयोग किए जाते हैं। बेंज़ीन डाइजियोनियम क्लोराइड फेनॉल के साथ अभिक्रिया करता है जिसमें फेनॉल अणु अपने पैरा स्थिति पर डाइजियोनियम लवण के साथ जुड़ता है और प-हाइड्रॉक्सीएजोबेंज़ीन बनता है। इस प्रकार की अभिक्रिया को क्लॉपिंग अभिक्रिया के रूप में जाना जाता है।

यह देखा जा सकता है कि, फेनॉल और एनिलीन के पैरा स्थिति डाइजियोनियम लवण के साथ जुड़ते हैं। यह अभिक्रिया इलेक्ट्रोफिलिक प्रतिस्थापन के माध्यम से चलती है।
(v) अमोनोलिज़ेशन
जब एक ऐल्किल या बेंजिल हैलाइड को एथेनॉलिक अमोनिया विलयन में अभिक्रिया कराई जाती है, तो यह एक न्यूक्लियोफिलिक स्थानांतरण अभिक्रिया में भाग लेता है जिसमें हैलोजन परमाणु को ऐमीनो ( - ${NH_2}$ ) समूह द्वारा प्रतिस्थापित कर दिया जाता है। इस प्रक्रिया में कार्बन-हैलोजन बंध के विघटन को अमोनोलिज़ेशन कहा जाता है।

अमोनियम लवण से मुक्त ऐमीन को एक मजबूत क्षारक के साथ उपचार द्वारा प्राप्त किया जा सकता है :
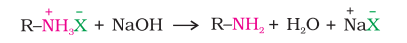
अमोनोलिज़ेशन का नुकसान यह है कि इसके द्वारा प्राथमिक, द्वितीयक और तृतीयक ऐमीन तथा एक चतुर्थक ऐमीनियम लवण के मिश्रण के निर्माण होता है। हालांकि, अमोनिया के बड़े अतिरिक्त मात्रा के साथ अभिक्रिया कराने से प्राथमिक ऐमीन मुख्य उत्पाद के रूप में प्राप्त होता है।

(vi) ऐसीटिलेशन
ऐसीटिलेशन (या ऐथेनॉयलेशन) एक अणु में ऐसीटिल समूह के प्रवेश की प्रक्रिया है।
अलिफैटिक और ऐरोमैटिक प्राथमिक और द्वितीयक ऐमीन अम्ल लवण, अनहाइड्राइड या एस्टर के साथ न्यूक्लियोफिलिक स्थानांतरण अभिक्रिया द्वारा ऐसीटिलेशन अभिक्रिया में भाग लेते हैं। इस अभिक्रिया में - ${NH_2} {Or}>{NH}$ समूह के हाइड्रोजन परमाणु को ऐसीटिल समूह द्वारा प्रतिस्थापित कर दिया जाता है, जिसके परिणामस्वरूप ऐमाइड के निर्माण होता है। अभिक्रिया के दौरान उत्पन्न ${HCl}$ को तुरंत हटाकर संतुलन को दाहिने ओर विस्थापित किया जाता है। इस अभिक्रिया को एक ऐमीन की तुलना में अधिक मजबूत क्षारक (जैसे पाइरिडीन) की उपस्थिति में कराया जाता है।


जब ऐमीन बेंज़ोइल क्लोराइड के साथ अभिक्रिया करते हैं, तो अभिक्रिया को बेंज़ोइल करण (benzoylation) के रूप में भी जाना जाता है।
उदाहरण के लिए,

(vii) गैब्रियल फ्थैलिमाइड संश्लेषण
गैब्रियल फ्थैलिमाइड संश्लेषण एलिफैटिक प्राथमिक ऐमीन के तैयार करने के लिए एक बहुत उपयोगी विधि है। इसमें फ्थैलिमाइड को एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ उपचार किया जाता है ताकि फ्थैलिमाइड के पोटैशियम लवण का निर्माण हो। इस लवण को आगे एक ऐल्किल हैलाइड के साथ गर्म किया जाता है, जिसके बाद क्षारीय हाइड्रोलिज़िस के अंतर्गत संगत प्राथमिक ऐमीन प्राप्त होता है।

13.8 निम्नलिखित परिवर्तन करें:
(i) नाइट्रोबेंज़ीन से बेंज़ोइक अम्ल
(ii) बेंज़ीन से m-ब्रोमोफेनॉल
(iii) बेंज़ोइक अम्ल से ऐनिलीन
(iv) ऐनिलीन से 2,4,6-ट्राइब्रोमोफ्लूओरोबेंज़ीन
(v) बेंजिल क्लोराइड से 2-फेनिलएथेनऐमीन
(vi) क्लोरोबेंज़ीन से p-क्लोरोएनिलीन
(vii) ऐनिलीन से p-ब्रोमोऐनिलीन
(viii) बेंज़ैमाइड से टॉलूईन
(ix) ऐनिलीन से बेंजिल ऐल्कोहल।
उत्तर दिखाएं
उत्तर
(i)

(ii)

(iii)

(iv)

(v)

(vi)

(vii)

(viii)

(ix)

13.09 निम्नलिखित अभिक्रियाओं में A, B और C के संरचना दीजिए:
(i) ${CH}_3 {CH}_2 {I} \xrightarrow{{NaCN}} {A} \xrightarrow[\text { आंशिक हाइड्रोलिसिस }]{{OH}^{-}} {B} \xrightarrow{{NaOH}+{Br}_2} {C}$
(ii) ${C}_6 {H}_5 {~N}_2 {Cl} \xrightarrow{{CuCN}} {A} \xrightarrow{{H}_2 {O} / {H}^{+}} {B} \xrightarrow[\Delta]{{NH}_3} {C}$
(iii) ${CH}_3 {CH}_2 {Br} \xrightarrow{{KCN}} {A} \xrightarrow{{LiAlH}_4} {~B} \xrightarrow[0^{\circ} {C}]{{HNO}_2} {C}$
(iv) ${C}_6 {H}_5 {NO}_2 \xrightarrow{{Fe} / {HCl}} {A} \xrightarrow[273 {~K}]{{NaNO}_2+{HCl}} {B} \xrightarrow[\Delta]{{H}_2 {O} / {H}^{+}} {C}$
(v) ${CH}_3 {COOH} \xrightarrow[\Delta]{{NH}_3} {~A} \xrightarrow{{NaOBr}} {B} \xrightarrow{{NaNO}_2 / {HCl}} {C}$
(vi) ${C}_6 {H}_5 {NO}_2 \xrightarrow{{Fe} / {HCl}} {A} \xrightarrow[273 {~K}]{{HNO}_2} {~B} \xrightarrow{{C}_6 {H}_5 {OH}} {C}$
उत्तर दिखाएं
Answer
(i) ${CH}_3 {CH}_2 {I} \xrightarrow{{NaCN}} {CH}_3 {CH}_2 {CN} \xrightarrow[\text { Partial hydrolysis }]{{OH}^{-}} {{CH}_3 {CH}_2CO{NH}_2} \xrightarrow{{NaOH}+{Br}_2} {{CH}_3 {CH}_2{NH}_2}$
(ii) ${C}_6 {H}_5 {~N}_2 {Cl} \xrightarrow{{CuCN}} {C_6H_5CN } \xrightarrow{{H}_2 {O} / {H}^{+}} {C_6H_5COOH} \xrightarrow[\Delta]{{NH}_3} {C_6H_5CONH_2}$
(iii) ${CH}_3 {CH}_2 {Br} \xrightarrow{{KCN}} {CH_3CH_2CN} \xrightarrow{{LiAlH}_4} {CH_3CH_2CH_2NH_2} \xrightarrow[0^{\circ} {C}]{{HNO}_2} {CH_3CH_2CH_2OH}$
(iv) ${C}_6 {H}_5 {NO}_2 \xrightarrow{{Fe} / {HCl}} {C_6H_5NH_2} \xrightarrow[273 {~K}]{{NaNO}_2+{HCl}} {C_6H_5N_2Cl} \xrightarrow[\Delta]{{H}_2 {O} / {H}^{+}} {C_6H_5OH}$
(v) ${CH}_3 {COOH} \xrightarrow[\Delta]{{NH}_3} {CH_3CONH_2} \xrightarrow{{NaOBr}} {CH_3NH_2} \xrightarrow{{NaNO}_2 / {HCl}} {CH_3OH}$
(vi) ${C}_6 {H}_5 {NO}_2 \xrightarrow{{Fe} / {HCl}} {C_6H_5NH_2} \xrightarrow[273 {~K}]{{HNO}_2} {C_6H_5N_2Cl} \xrightarrow{{C}_6 {H}_5 {OH}} {C_6H_5OH}$
13.10 एक औषधीय यौगिक ’ ${A}$ ’ के जलीय अमोनिया के साथ उपचार एवं गरम करने पर यौगिक ’ ${B}$ ’ बनता है, जिसे गरम करने पर ${Br_2}$ एवं ${KOH}$ के साथ एक यौगिक ’ ${C}$ ’ बनता है, जिसका अणुसूत्र ${C_6} {H_7} {~N}$ है। यौगिक ${A}, {B}$ एवं ${C}$ के संरचना एवं IUPAC नाम लिखिए।
उत्तर दिखाएं
उत्तर
दिया गया है कि अणुसूत्र ${C_6} {H_7} {~N}$ वाला यौगिक ’ ${C}$ ’ ब्रोमीन और कॉपर अम्ल (${Br_2}$ और ${KOH}$) के साथ गर्म करने पर बनता है। यह एक हॉफमैन ब्रोमएमाइड अपघटन अभिक्रिया है। अतः, यौगिक ’ ${B}$ ’ एमाइड है और यौगिक ’ ${C}$ ’ एमीन है। अणुसूत्र ${C_6} {H_7} {~N}$ वाला एकमात्र एमीन एनिलीन है, $\left({C_6} {H_5} {NH_2}\right)$।

अतः, यौगिक ‘B’ (जिससे ’ ${C}$ ’ बनता है) बेंज़े एमाइड होना चाहिए, $\left({C_6} {H_5} {CONH_2}\right)$।

इसके अतिरिक्त, बेंज़े एमाइड अम्लीय अमोनिया के साथ गर्म करने पर बनता है। अतः, यौगिक ‘A’ बेंज़े एसिड होना चाहिए।

बेंज़े एसिड
दिए गए अभिक्रियाओं को निम्नलिखित समीकरणों की सहायता से समझा जा सकता है:

13.11 निम्नलिखित अभिक्रियाओं को पूरा करें:
(i) ${C_6} {H_5} {NH_2}+{CHCl_3}+$ ऐल्कोहली ${KOH} \rightarrow$
(ii) ${C_6} {H_5} {~N_2} {Cl}+{H_3} {PO_2}+{H_2} {O} \rightarrow$
(iii) ${C_6} {H_5} {NH_2}+{H_2} {SO_4}$ (केंद्रित) $\rightarrow$
(iv) ${C_6} {H_5} {~N_2} {Cl}+{C_2} {H_5} {OH} \rightarrow$
(v) ${C_6} {H_5} {NH_2}+{Br_2}({aq}) \rightarrow$
(vi) ${C_6} {H_5} {NH_2}+\left({CH_3} {CO}\right)_{2} {O} \rightarrow$
(vii) ${C} _{6} {H} _{5} {~N} _{2} {Cl} \xrightarrow[\text { (ii) } {NaNO} _{2} / {Cu}, \Delta]{\left(\text { i) } {HBF} _{4}\right.}$
उत्तर दिखाएं
Answer
(i)
$ \begin{aligned} & {C}_6 {H}_5 {NH}_2+{CHCl}_3+3 {KOH} \rightarrow \underset{\text { Phenyl isocyanide }}{{C}_6 {H}_5 {NC}} +3 {KCl}+3 {H}_2 {O} \end{aligned} $
(ii) $\underset{\substack{\text{Benzenediazonium}\\ \text{chloride}}}{{C_6} {H_5} {~N_2} {Cl}}+{H_3} {PO_2}+{H_2} {O} \rightarrow \underset{\text{Benzene}}{{C_6} {H_6}}+{N_2}+{H_3} {PO_3}+{HCl}$
(iii)

(iv) $ \underset{\substack{\text{Benzenediazonium}\\ \text{chloride}}}{{C_6} {H_5} {N_2} {Cl}}+\underset{\text{Ethanol}}{{C_2} {H_5} {OH}} \rightarrow \underset{\text{Benzene}}{{C}_6 {H}_6}+ \underset{\text{Ethanal}}{{CH}_3 {CHO}}+{N_2}+{HCl} $
(v)

(vi)

(vii)

13.12 क्यों ऐरोमैटिक प्राथमिक ऐमीन गैबरियल फ्थैलिमाइड संश्लेषण द्वारा नहीं बनाए जा सकते?
उत्तर दिखाएं
Answer
गैबरियल संश्लेषण प्राथमिक ऐमीन के निर्माण के लिए उपयोग किया जाता है। फ्थैलिमाइड एथेनॉलिक पोटैशियम हाइड्रॉक्साइड के साथ उपचार के बाद फ्थैलिमाइड के पोटैशियम लवण का निर्माण करता है जिसे एल्किल हैलाइड के साथ गर्म करके तथा अम्लीय हाइड्रॉलिज़िस के बाद संगत प्राथमिक
amine.

अर्थवत्ता प्राथमिक ऐमीन इस विधि से तैयार नहीं किए जा सकते हैं क्योंकि ऐरिल हैलाइड फथलिमाइड द्वारा बनाए गए एनियन के साथ न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया नहीं करते हैं।

अतः, अर्थवत्ता प्राथमिक ऐमीन इस प्रक्रिया द्वारा तैयार नहीं किए जा सकते हैं।
13.13 (i) अर्थवत्ता एवं (ii) अलिफैटिक प्राथमिक ऐमीन के नाइट्रस अम्ल के साथ अभिक्रिया लिखिए।
उत्तर दिखाएं
उत्तर
(i) अर्थवत्ता ऐमीन, नाइट्रस अम्ल (जो ${NaNO_2}$ एवं एक खनिज अम्ल जैसे ${HCl}$ के साथ स्थानांतरित रूप से बनाया जाता है) के साथ 273 - $278 {~K}$ पर अभिक्रिया करते हैं ताकि स्थायी अर्थवत्ता डाइजोनियम लवण बने, अर्थात, ${NaCl}$ एवं ${H_2} {O}$।

(ii) अलिफैटिक प्राथमिक ऐमीन, नाइट्रस अम्ल (जो ${NaNO_2}$ एवं एक खनिज अम्ल जैसे ${HCl}$ के साथ स्थानांतरित रूप से बनाया जाता है) के साथ अभिक्रिया करते हैं ताकि अस्थायी अलिफैटिक डाइजोनियम लवण बने, जो आगे चलकर एल्कोहल एवं ${HCl}$ बनाते हैं एवं ${N_2}$ गैस के उत्सर्जन के साथ।

13.14 निम्नलिखित के लिए प्रत्येक के लिए संभावित स्पष्टीकरण दीजिए:
(i) क्यों ऐमीन तुलनात्मक अणुभार वाले अल्कोहल की तुलना में कम अम्लीय होते हैं?
(ii) क्यों प्राथमिक ऐमीन तृतीयक ऐमीन की तुलना में उच्च क्वथनांक रखते हैं?
(iii) क्यों अलिफैटिक ऐमीन ऐरोमैटिक ऐमीन की तुलना में अधिक क्षारक होते हैं?
उत्तर दिखाएँ
उत्तर
(i) ऐमीन्स तुलनात्मक अणुभार वाले अल्कोहल की तुलना में कम अम्लीय होते हैं। इसका कारण नीचे बताया गया है:
- ऐमीन्स एक प्रोटॉन खोकर ऐमाइड आयन बनाते हैं। अल्कोहल एक प्रोटॉन खोकर ऐल्कॉक्साइड आयन बनाते हैं।
- ऐमाइड आयन के निर्माण: ${R}-{NH}_2 \longrightarrow {R}-{NH}^{-}+{H}^{+}$
- ऐल्कॉक्साइड आयन के निर्माण: ${R}-{OH} \longrightarrow {R}-{O}^{-}+{H}^{+}$
- ऑक्सीजन नाइट्रोजन की तुलना में अधिक विद्युत ऋणात्मक होती है, इसलिए ऐल्कॉक्साइड आयन ऐमाइड आयन की तुलना में अधिक स्थायी होती है। इसलिए, अल्कोहल ऐमीन्स की तुलना में अधिक अम्लीय होते हैं।
(ii) प्राथमिक ऐमीन्स में नाइट्रोजन परमाणु दो हाइड्रोजन परमाणु रखते हैं जो विस्तारित अंतराणु ${H}$-बंधन के कारण होते हैं। तृतीयक ऐमीन्स में नाइट्रोजन परमाणु कोई भी हाइड्रोजन परमाणु नहीं रखते हैं और हाइड्रोजन बंधन संभव नहीं होता।
इसलिए, प्राथमिक ऐमीन्स तृतीयक ऐमीन्स की तुलना में अधिक क्वथनांक रखते हैं।

भाग (iii) : अलिफैटिक ऐमीन्स औषधीय ऐमीन्स की तुलना में अधिक क्षारक होते हैं, इसके कारण नीचे दिए गए हैं: (a) औषधीय ऐमीन्स के नाइट्रोजन परमाणु के अकेले इलेक्ट्रॉन वाले वृत्त के $\pi$-बंध युग्मों के साथ संयोजन में शामिल होते हैं जैसे कि नीचे दिखाया गया है

(b) एनिलीनियम आयन जो एक प्रोटॉन ग्रहण करके बनता है, अनुनाद द्वारा कम स्थायी होता है। बेंजीन वलय के $-{R}$ प्रभाव के कारण, औषधीय ऐमीन्स में नाइट्रोजन परमाणु पर इलेक्ट्रॉन कम उपलब्ध होते हैं। इसलिए, औषधीय ऐमीन्स में नाइट्रोजन परमाणु पर इलेक्ट्रॉन को आसानी से दान करना संभव नहीं होता।
हम जानते हैं कि अधिक अनुनाद संरचनाएं, अधिक स्थायिता होती है। इसलिए आप अनुमान लगा सकते हैं कि एनिलीन (पांच अनुनाद संरचनाएं) एनिलीनियम आयन की तुलना में अधिक स्थायी होता है। इसलिए, एनिलीन या अन्य औषधीय ऐमीन्स के प्रोटॉन ग्रहण क्षमता या क्षारकीय प्रकृति के बारे में बताया जा सकता है।
कम होगा।
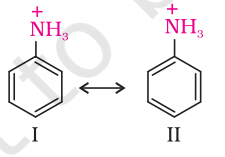
इसलिए, एनिलीन ऐल्किल ऐमीन की तुलना में कम क्षारक होता है, जहाँ $+I$ प्रभाव नाइट्रोजन पर इलेक्ट्रॉन घनत्व को बढ़ाता है।





